Blog

Naziv: askorbinska kiselina, acidum ascorbicum, engleski: ascorbic acid, francuski: acide ascorbique, nemački: Askorbinsäure
Poreklo naziva: onaj koji leči skorbut
Vitamin C ili askorbinska kiselina nije samo antioksidans. On učestvuje u procesima poput stvaranja vlakna kolagena, i nastanka adrenalina i noradrenalina potrebnih za funkciju nervnog sistema. Vitamin C učestvuje i u kontroli gena. Ima ga najviše u svežem voću i povrću, i potrebno nam je 75-120 miligrama dnevno. Termička obrada hrane smanjuje njegov sadržaj, ali ga kuvanje na pari najbolje očuva. Kome je potreban vitamin C kao suplement? To su aktivni i pasivni pušači, kojima je u proseku potrebno 35 miligrama više, kao i ljudi koji konzumiraju malo sirovog voća i povrća. Osobe sa zapaljenskim bolestima creva, kao i onkološki pacijenti sa nekim gastrointestinalnim tumorima, takođe mogu imati rizik od njegovog nedostatka. Možete ga koristiti do dva grama dnevno. Drugi lekovi se mogu koristiti sa vitaminom C, a nuspojave su retke. Vitamin C može smanjiti rizik od prehlade kod ljudi koji se bave intenzivnom fizičkom aktivnošću, a ima i nekoliko potencijalnih ciljanih primena kod drugih bolesti. Vitamin C u suplementima ne smanjuje rizik od malignih tumora i kardiovaskularnih bolesti, za razliku od hrane, voća i povrća, koja je njime bogata. Takva hrana obiluje i drugim nutrijentima, a ne samo vitaminom C. Rizik od nastanka kamena u urinarnom traktu zbog njegove produžene upotrebe verovatno je mali, pogotovo kod žena. Ne postoje veće razlike u delotvornosti raznih oblika vitamina C na tržištu.

Istorija otkrića vitamina C
Teški nedostatak vitamina C naziva se skorbut, i bio je poznat ne samo među mornarima, već je bio veliki problem u širokoj populaciji u doba gladi. Lečenje skorbuta opisao je James Lind u XVIII veku, ali on nije bio prvi koji je koristio pomorandže i limun za lečenje skorbuta. Otkriće vitamina C dogodilo se tek u XX veku. Albert Szent-Györgyi prvi je izolovao vitamin C i opisao njegovu antioksidativnu (reduktivnu) funkciju.
- 1,2 litre jabukovače (hard apple cider, alkoholno piće napravljeno od jabuka)
- 25 kapi sumporne kiseline razblažene u vodi, tri puta dnevno
- 18 ml sirćeta tri puta dnevno
- 3 decilitra morske vode
- 2 pomorandže i limun kroz šest dana
- 4 mililitra medicinske paste spravljene od senfa, belog luka, korena rena, Peru balzama i smirne smole u ječmenom soku zakiseljenom tamarindom, sa dodatkom kalijum hidrogen-tartarata (so vinske kiseline).

Biološka funkcija vitamina C, metode određivanja njegovog nedostatka i skorbut
Vitamin C je antioksidans i kofaktor nekoliko enzima koji učestvuju u stvaranju hormona, kolagena, adrenalina i noradrenalina u nervnom sistemu, kao i stvaranju karnitina, koji omogućuje stvaranje energije u ćelijama. Vitamin C učestvuje i u kontroli gena. Težak nedostatak vitamina C uzrokuje bolest skorbut, koja je smrtonosna ako se ne leči. Manjak vitamina C može se odrediti laboratorijskim merenjem u plazmi ili belim krvnim zrncima.
Vitamin C je kofaktor nekoliko enzima u ljudskom telu [9-11]:
- prolil-3 hidroksilaza, prolil-4 hidroksilaza i lizil hidroksilaza. Oni oksidišu aminokiseline prolin i lizin, a taj proces je neophodan u biosintezi raznih kolagena, kao i C1q protein komplementa, proteina koji je važan deo imunološkog sistema. Kao kofaktor ovi enzimi koriste i gvožđe. Simptomi skorbuta- krvarenje iz desni, kožne manifestacije i bolesti drugih vezivnih tkiva, kao i smanjena imunološka odbrana, mogu se objasniti baš nedostatkom delovanja ovih enzima.
- 4-hidroksifenil piruvat dioksigenaza, koja učestvuje u razgradnji aminokiseline tirozina.
- dopamin-beta monooksigenaza koji učestvuje u biosintezi adrenalina i noradrenalina iz dopamina. Kao kofaktor ovaj enzim koristi i bakar. Kako su adrenalin i noradrenalin vrlo bitni za aktivnost, deo simptoma skorbuta („lenjost“, usporenost, nemotivisanost), može se objasniti nedostatkom ovih važnih neurotransmitera.
- 6-N-trimetil-L-lizin hidroksilaza i gama-butirobetain hidroksilaza enzimi su koji učestvuju u biosintezi karnitina. Karnitin je važan faktor u razgradnji masnih kiselina i dobijanju energije. Kao kofaktor ovi enzimi koriste gvožđe. Manjak karnitina barem delom pridonosi nastanku umora kao simptoma skorbuta.
- peptidil glicin alfa-amidirajuća monoksigenaza (PAM), koja obavlja proces amidacije (pretvaranja u amid) raznih peptida na mestu pozicije aminokiseline glicina, što je neophodno za njihovu biološku funkciju. Kao kofaktor koristi i bakar. PAM enzim je nužan za nastanak niza peptida, poput alfa-melanocitnog hormona.
- HIF (Hypoxia-inducible factor-proline) dioksigenaza (HIF hidroksilaza), koja potiče razgradnju HIF-a. HIF je transkripcijski faktor koji omogućava telu odbranu od hipoksije i oksidativnog stresa. Zanimljivo, vitamin C u ovom je slučaju kofaktor enzima koji smanjuje aktivnost zaštitnog proteina i potencijalni lekovi koji smanjuju ovaj proces razvijani su za lečenje bolesti koje pogađaju srce i bubrege.
Dakle, vitamin C nije samo antioksidans, već faktor aktivnosti enzima koji su čoveku važni svakoga dana.
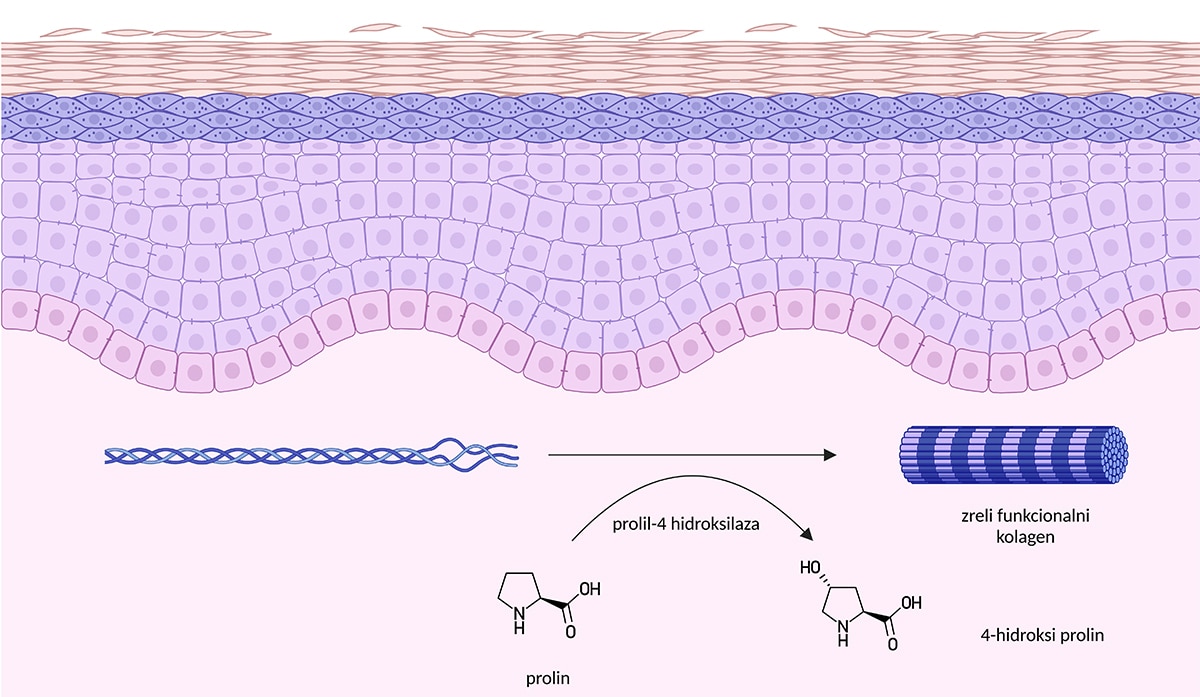
4-hidroksilacija aminokiseline prolina neophodna je za nastanak funkcionalnog molekula kolagena, a ona zavisi od vitamina C. U tom procesu vitamin C se oksidira, a nastaje 4-hidroksiprolin.
Osim ovih „klasičnih“ biohemijskih uloga, tek je nedavno otkrivena i druga uloga vitamina C u epigenetici. Kofaktor je enzima koji uklanjaju metilnu skupinu DNK i histona, proteina vezanih za DNK. To su enzimi poput TET (ten eleven translocase), kao i histon demetilaze s Jumonji domenama (Jumonji domain-containing histone demethylases). Na taj način učestvuju u regulaciji ekspresije gena [12].
Nabrojeni fiziološki učinci vitamina C drugačiji su od uobičajene percepcije vitamina C kao antioksidansa. Sve su to redom precizne biohemijske reakcije daleko od klasičnih reakcija delovanja na reaktivne kiseonikove vrste (ROS), odnosno na pro-oksidanse koji nastaju u organizmu. Postavlja se pitanje- u kojoj je meri vitamin C realan fiziološki antioksidans koji ne zavisi od specifičnih enzimskih reakcija? Vitamin C je zaista antioksidans i u prehrambenoj industriji, koji štiti hranu od oksidativnog kvarenja. Treba biti oprezan u interpretaciji brojnih objavljenih in vitro studija. Realni biološki efekti očekuju se u koncentracijama od 10 do 100 µmol/l i veliko je pitanje koje je biološko značenje ispitivanja vrlo velikih koncentracija koje prelaze 1 mmol/l. Već je u XX veku nastalo je veliko razočaranje zbog kliničkog neuspeha vitamina C u bolestima u kojima učestvuju pro-oksidansi kao što su slobodni radikali. Postavilo se heretičko pitanje: što ako vitamin C uopšte nije fiziološki antioksidans?
Ipak, čini se da on igra ulogu antioksidansa uz brojne druge sisteme zaštite koji postoje u telu. Vitamin C lako oksidiše i prvo nastaje radikal askorbinske kiseline. Veliki broj radikala vrlo je nestabilan i oni reaguju sa drugim molekulima. Radikal vitamina C je neobično stabilan i može postojati više minuta. Nakon još jedne oksidacije nastaje dehidroaskorbinska kiselina (pogledati: Apsorpcija, distribucija, metabolizam, izlučivanje). U tom procesu askorbinska kiselina reducira ROS-ove. Neutrofili su ćelije u kojima je antioksidativni učinak vitamina C verovatno realan. Neutrofili stvaraju vrlo visoke nivoe ROS-ova koje koriste kao hemijsko oružje, u borbi s mikroorganizmima u procesu koji na engleskom nazivamo „oxidative burst“. Oni su štetni ne samo za mikroorganizme, nego i za naše ćelije. Neutrofili nakupljaju velike količine vitamina C, koji im verovatno služi kao zaštita od ROS-ova koje sami stvaraju [13]. U dokazivanju fiziološke antioksidativne funkcije problem nam predstavljaju markeri oksidativnog stresa kod ljudi, poput malondialdehida, 8-oksogvanina, lipidnih peroksida i 8-izo-prostaglandin-F2α. Rezultati kliničkih studija su različiti, i ne potvrđuju sve studije efekat vitamina C na navedene markere [14-21]. Delotvornost zavisi od puno faktora, uključujući i odabrane grupe u studijama, ali, postavlja se pitanje koliko su takvi markeri relevantni za procenu fiziološke funkcije vitamina C kao antioksidansa. Verovatno učestvuje i u redukciji vitamina E [22]. Vitamin C je verovatno fiziološki antioksidans, ali ne treba precenjivati njegovu antioksidativnu ulogu u odnosu na druge fiziološke mehanizme zaštite tela od ROS-ova [10, 23, 24]. Vitamin C je antioksidans i u nama evolucijski udaljenim biljkama [25].
Vitamin C nije vitamin za sve životinjske vrste. Brojne životinjske vrste mogu stvoriti vitamin C u nekoliko enzimskih reakcija iz glukoze. Ali, neke su vrste izgubile ključni enzim nazvan GULO (L-gulono gama-lakton oksidaza), koji je zadužen za poslednji korak u stvaranju vitamina C [26, 27]. Te vrste su raznolike, od primata skupine Haplorhini, što uključuje i čoveka, deo slepih miševa, riba i morsku prasad. Gubitak stvaranja vitamina C dogodio se nezavisno više puta u evoluciji i nije jasna evolucijska prednost koju takav gubitak donosi.
Produženi manjak vitamina C uzrokuje tešku bolest skorbut [28]. Obično se javlja 8-12 nedelja nakon izostanka vitamina C u ishrani (manje od 10 mg dnevno), sa simptomima umora, mučnine, iritabilnosti i anoreksije. Prvi znakovi mogu se katkad javiti i ranije. Javljaju se oticanje i krvarenje iz zubnog mesa, modrice i malena krvarenja u koži zbog smanjenog stvaranja kolagena. Vremenom dolazi do oticanja nogu, a krvarenja se češće javljaju u nogama. Kosti mogu postati krhke, a javlja se i bol u zglobovima. Oticanje celog tela, krvarenje, raspad crvenih krvnih zrnaca i žutica mogu uzrokovati smrt. Ukoliko se ne leči, skorbut je smrtonosan. Skorbut se leči sa 500-1000 mg vitamina C dnevno, a kroz prva tri dana doza se može povećati na 2 grama.
Vitamin C može se određivati direktno u plazmi ili leukocitima. U plazmi normalno nalazimo 0,4 do 1,5 mg/dl (23-84 µmol/l). Vrednosti od 0,2 do 0,4 mg/dl (11.4-23 µmol/l) su marginalni deficit ili suboptimalna nivo, a nivo manji od 0,2 mg/dl ukazuje na teški nedostatak. Vitamin C može se određivati u leukocitima, gdje se nalazi u većoj koncentraciji. U skorbutu koncentracija gotovo pada na nulu, 0-7 mg/dl ukazuje na ozbiljniji nedostatak, a nivo veći od 15 mg/dl ukazuje na dovoljan nivo u telu.
Ko ima rizik od nedostatka vitamina C?
- pasivni i aktivni pušači
- pacijenti s lošom apsorpcijom hrane, npr. zbog zapaljenskih bolesti creva
- alkoholičari
- stariji ljudi i ljudi sa oskudnom i monotonom ishranom
- ljudi oboleli od anoreksije, ortoreksije i bulimije
- siromašniji ljudi koji konzumiraju malo voća i povrća
- deca hranjena samo prokuvanim kravljim mlekom
- neki pacijenti s dijabetesom tipa I

Apsorpcija, distribucija, metabolizam, izlučivanje
Vitamin C ne apsorbuje se spontanim prolaskom kroz ćelije creva (difuzijom), već taj proces omogućavaju transportni proteini. Ne postoji pravilo da će veća doza izazvati proporcionalan rast u krvi, jer je aktivni transport u sistemu za varenje saturabilan (lako se zasiti). Jednokratne doze veće od 500 mg manje se efikasno apsorbuju. Vitamin C se nakuplja u tkivima poput mozga i nadbubrežne žlezde, ali i u belim krvnim zrncima. Bubrezi su vrlo važan organ u regulaciji, jer izuzetno lako izlučuju višak vitamina C. U slučaju nedostatka vitamina C bubrezi ga „štede“, odnosno reapsorbuju (vraćaju) u krv. Nedostatak vitamina C u ishrani neće odmah izazvati posledice poput skorbuta, jer ga telo može skladištiti u tkivima tokom nekoliko nedelja. Izuzetno visoke koncentracije u krvi mogu se postići samo lekovima koji se daju u venu (intravenskim lekovima). Vitamin C se razgrađuje (metabolizuje) u šećere, oksalnu kiselinu, kao i niz drugih jedinjenja. Premda se vitamin C razgrađuje u oksalnu kiselinu, normalne suplementacijske doze unutar sigurnih granica verovatno ne povećavaju rizik od nastanka kamena u bubrezima i mokraćnoj bešici.
Gubitkom sposobnosti stvaranja vitamina C postali smo zavisni od njegovog unosa hranom. Zbog toga smo razvili vrlo delotvoran i specifičan način njegove apsorpcije u sistemu za varenje. Vitamin C u hrani postoji u dva oblika:
- redukovani oblik, askorbinska kiselina
- oksidovani oblik, dehidroaskorbinska kiselina
Vitamin C je mali molekul koji je u sistemu za varenje uglavnom u obliku anjona, osim u kiselom sadržaju želuca. Zbog toga je mogućnost apsorpcije pasivnom difuzijom kroz membranu malo verovatna. Askorbinska i dehidroaskorbinska kiselina pokazuju sličnu bioraspoloživost, što je mudro sa evolucijskog aspekta. Dehidroaskorbinska kiselina čini mali udeo ukupnog vitamina C u krvi, ali je može biti više u hrani.
Vitamin C se apsorbuje u crevima kroz čak pet transportera [29]:
- SVCT1 i SVCT2 (Sodium-Dependent vitamin C transporter), koji omogućavaju apsorpciju redukovanog oblika. Kao što im ime govori, menjaju natrijum za molekul askorbinske kiseline. SVCT1 je najviše prisutan na ćelijama epitela creva i verovatno je najbitniji za prvi korak u apsorpciji.
- GLUT1, GLUT 3 i GLUT8 transporteri (za šećere heksoze poput glukoze), kroz koje se apsorbuje oksidovani oblik.
Ulazak u enterocit predstavlja tek polovinu puta apsorpcije i očito mora postojati transporter koji služi transportu iz enterocita u krvotok. Za sada nije sigurno koji je to protein. Niz in vitro studija ukazivao je na mogućnost da glukoza ometa apsorpciju dehidroaskorbinske kiseline, a flavonoidi iz voća i povrća smanjuju apsorpciju askorbinske kiseline, ali studije na ljudima nisu zasad potvrdile in vitro opažanja.
Redukovani oblik vitamina C, askorbinska kiselina, apsorbira se pomoću SVCT1 transportera. U tom procesu askorbinska kiselina menja se sa natrijumom, što znači da natrijum izlazi iz ćelije u sadržaj creva, dok vitamin C ulazi u crevnu ćeliju.

Većina vitamina C u krvotoku nalazi se u obliku redukovane askorbinske kiseline s prosečnom koncentracijom u plazmi od 50-70 µmol/l. Pomoću SVCT2 dolazi do nakupljanja vitamina C u tkivima u daleko većem nivou nego u plazmi. SVCT2 ima snažniji afinitet vezanja askorbinske kiseline od SVCT1 transportera. U plućima i jetri nalazimo oko 1 mmol/l, a u mozgu i nadbubrežnoj žlezdi čak do 10 mmol/l. Takav nivo verovatno reflektuje potrebe tkiva za enzimskim reakcijama. Crvena krvna zrnca nemaju SVCT transportere i nivo vitamina C u njima sličan je nivou u plazmi, dok leukociti, neutrofili i monociti sadrže oko 14 puta veću koncentraciju od krvne plazme [30]. Mozak je privilegovani organ i čak i u snažnom manjku poput skorbuta, telo u mozgu zadržava visok nivo vitamina C, nauštrb drugih organa. Telo sadrži oko 1,5 grama zaliha vitamina C u telu, a prema procenama, skorbut se javlja kada zalihe padnu ispod 350 mg. Zalihe traju relativno kratko i u slučaju teškog nedostatka u ishrani iscrpe se u roku 4-12 nedelja, što i odgovara istorijskom skorbutu kod mornara [28].
Redukovani oblik vitamina C, askorbinska kiselina, u fiziološkim se procesima pretvara u dehidroaskorbinsku kiselinu. Bili bismo u velikom problemu kada bi priča vitamina C stala na ovom koraku, jer bi gubitak bio prebrz. Srećom, naše telo ima sposobnost regeneracije, odnosno redukcije dehidroaskorbinske kiseline pomoću enzima glutation i dihidroaskorbat reduktaze. Gotovo neiscrpan izvor vlastitog antioksidansa glutationa koji sami stvaramo, za razliku od vitamina C, omogućava neprestano recikliranje vitamina C i relativno mali gubitak tokom dana.
Oksidirani oblik vitamina C, dehidroaskorbinska kiselina, može se redukovati pomoću našeg vlastitog antioksidansa glutationa. Na taj način štedimo vitamin C.

Oksidirani oblik vitamina C, dehidroaskorbinska kiselina, može se redukovati pomoću našeg vlastitog antioksidansa glutationa. Na taj način štedimo vitamin C.

Na koji način uklanjamo vitamin C iz organizma? Postoje dva nezavisna puta [31]:
- bubrezima kroz urin
- katabolizmom (razgradnjom)
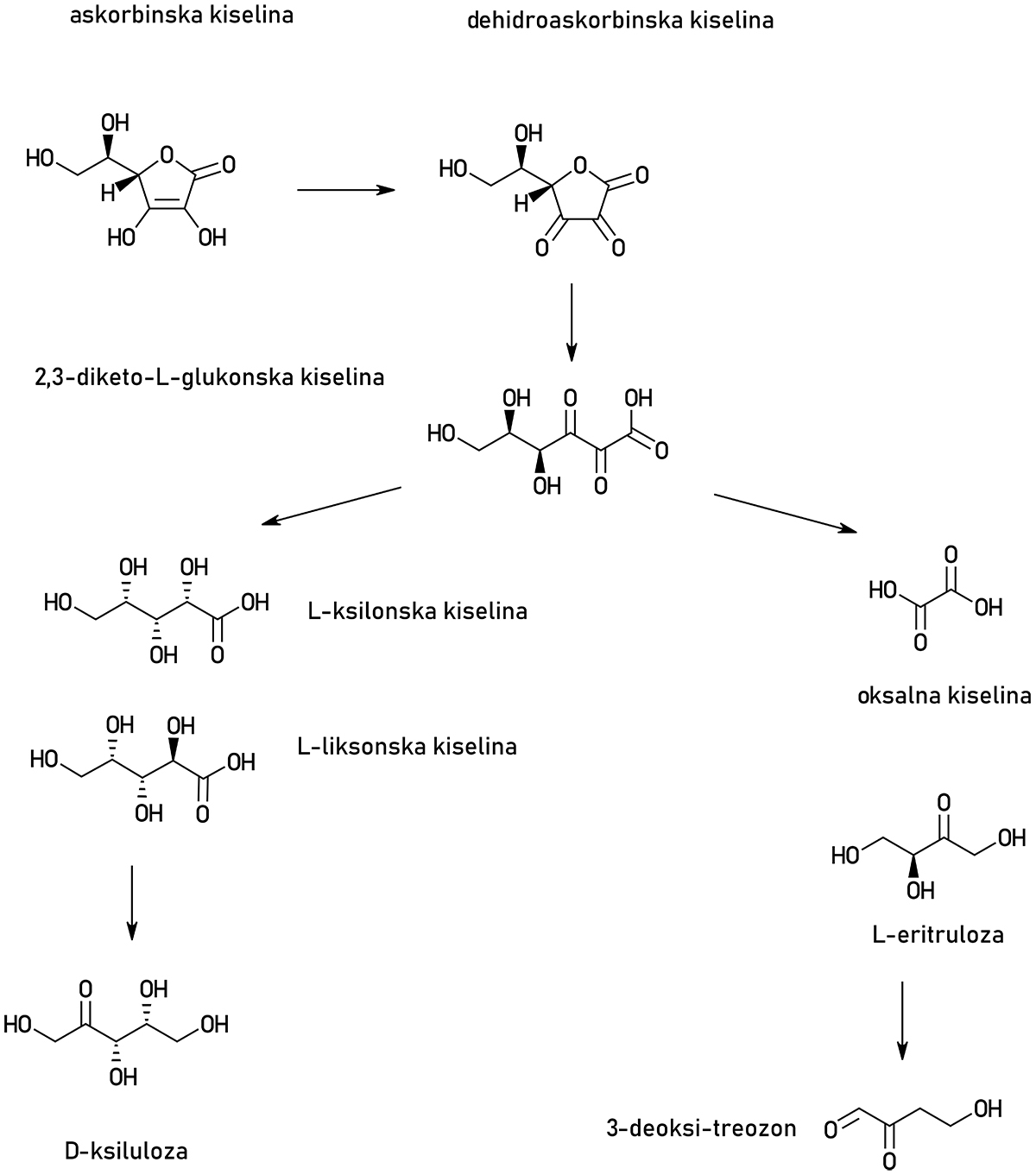
Razgradnja askorbinske kiseline započinje od dehidroaskorbinske kiseline iz koje nastaje 2,3-diketo-L-gulonat. Iz tog molekula mogu nastati dve kiseline, L-ksilonska i L-liksonska kiselina. One se mogu redukovati u šećer D-ksilulozu i na taj način se iskoristiti kao šećer kroz ciklus pentoza fosfata. Iz 2,3-diketo-L-gulonata mogu nastati šećer eritruloza i oksalna kiselina. Drugi produkti mogu nastati iz eritruloze, poput 3-deoksitreozona. Oksalna kiselina izlučuje se bubrezima, dok se drugi produkti mogu u određenoj meri i vezati za proteine Maillardovom reakcijom, i tek naknadno izlučiti iz organizma.
Višak vitamina C izlučujemo bubrezima ili razgrađujemo na nekoliko molekula. Šećere poput ksiluloze koristimo u metabolizmu, a oksalnu kiselinu izlučujemo bubrezima.


Višak vitamina C izlučujemo bubrezima ili razgrađujemo na nekoliko molekula. Šećere poput ksiluloze koristimo u metabolizmu, a oksalnu kiselinu izlučujemo bubrezima.
Zbog razgradnje vitamina C do oksalne kiseline postoji strah od povećanja rizika od nastanka kamena u urinarnom traktu. Rezultati studija nisu dali jasan odgovor [32-36]. Velika metaanaliza iz 2019. godine nas zbunjuje. Autori su učesnike studije rasporedili u četiri kategorije doziranja: 250-499 mg/dan, 500-999 mg/dan, 1000-1499 mg/dan, >1500 mg/dan, po polu. Kod žena ne postoji povećani rizik, dok kod muškaraca postoji, ali samo u dnevnim dozama 250-499 mg/dan i 1000-1499 mg/dan. Paradoksalno, povećani rizik nije pronađen kod ljudi koji su koristili vitamin C u dozama 500-999 mg/dan i >1500 mg/dan. Ovaj paradoks da kod najviših doza suplementacije postoji manji rizik nego kod najmanjih doza nema fiziološko objašnjenje, i dovodi u pitanje kauzalnost (uzročnost), i poziva na daleko veće studije [37].
Bubrezi jednostavno učestvuju u kontroli nivoa vitamina C u krvi. Kao mali polarni molekul, vitamin C se u glomerulu bubrega lako filtrira iz krvi. Zbog promene pH, u primarnom urinu može biti 1500 puta više vitamina C u odnosu na krv. Reapsorpcija (ponovni povratak u krvotok) nije spontani proces (difuzija), već je zavisna od SVCT1 transportera, koji ga „pumpa“ natrag u krvotok. Što je više vitamina C, pada reapsorpcija putem SVCT1 i na taj način organizam vrlo brzo uklanja višak iz tela. Intravenskom primenom vrlo visokih doza vitamina C dolazi do brzog izlučivanja bez reapsorpcije u krv [29].
Nakon oralne primene manje doze do 200 mg se dobro apsorbuju i bioraspoloživost doseže i više od 90 posto [30]. Ukoliko se koristi doza od 100 mg, ne dolazi do izlučivanja urinom. Kao što je i očekivano za molekul koji se apsorbuje aktivnim transportom, veće oralne doze ne izazivaju linearni porast u krvi i to se počinje videti već na dozama od 500 mg. Doza veća od 1 grama manje je od 50 posto bioraspoloživa i dolazi do povećanja izlučivanja askorbinske kiseline i oksalata urinom [30, 38]. Uobičajena koncentracija u krvi nakon oralne suplementacije iznosi 70–80 µmol/l i povećanje oralne doze do 1-2 grama ne povećava taj nivo. Više gramske doze mogu kratkotrajno povećati nivo u krvi. Oralna doza od 4 grama podiže nivo do oko 170 µmol/l [39]. Nije jasno postoji li ikakva zdravstvena prednost povišenja nivoa iznad 70–80 µmol/l kod oralnih preparata. Budući da na nivo vitamina C utiče više faktora (unos, aktivni transport, fizičke zalihe, izlučivanje i reapsorpcija u bubrezima), farmakokinetički parametri nisu jednostavni. Poluvreme života nižih oralnih doza meri se u danima, dok nivoi iznad 70 µmol/l nakon oralnog doziranja imaju poluvreme života do samo 30 minuta [40].
Intravenskom primenom zaobilazi se aktivni transport u sistemu za varenje, pa se dostiže daleko veća koncentracija u krvi. Sve do doze od 70g/m2 dolazi do linearnog porasta koncentracije u krvi do oko 50 mmol/L. Čini se da ovako visoke doze ne menjaju metabolizam i distribuciju vitamina C, ali moguće je da u nekim tkivima, poput tumorskih, vitamin C izaziva porast vodonik peroksida [41]. Poluvreme života nakon intravenske primene je oko 2 sata, što znači da se koncentracija u krvi smanjuje na fiziološki nivo u roku od 16 sati [42, 43].

Koliko nam treba vitamina C i koji faktori utiču na njega?
Ljudskom telu potrebno je 75-120 mg vitamina C dnevno. Dojilje imaju najveću potrebu za vitaminom C, a pušači trebaju barem 35 miligrama više svaki dan. Bez nadzora stručne osobe smemo uzimati do dva grama dnevno. Postoje mišljenja kako su optimalne dnevne doze i veće od 120 mg, i iznose oko 200 mg, pogotovo kod starijih ljudi. Niz faktora utiče na dovoljan unos vitamina C. Ishrana je ključni faktor, ali na to utiču i godišnja doba, način kuvanja, kao i delimično i genetske razlike između ljudi.
Unos vitamina C je neophodan za život i to je zahtev naše fiziologije. To je apsolutni medicinski konsenzus. Velike kontroverze o stvarnim potrebama za vitaminom C traju i dan-danas.
Prve kontroverze nastale su zbog razvoja biohemije i proučavanja vrsta koje same stvaraju vitamin C. Čovek i primati, morska prasad i znatan deo riba su primeri vrsta koje su izgubile enzim L-galanktolakton oksidazu, enzim kojim se deo glukoze pretvara u vitamin C. Znatan deo vrsta sačuvao je taj enzim. U starim ispitivanjima kod eksperimentalnih životinja pokazalo se kako svinja sintetizuje 10 mg/kg vitamina C, a pacov 200 mg/kg. Na osnovi tih podataka Linus Pauling je tvrdio kako čoveku trebaju gramske doze vitamina C dnevno. Takve je doze gotovo nemoguće dobiti ishranom, i Linus i njegov tim ignorisali su jednostavnu evolucijsku logiku. Da nam zaista trebaju takve količine koje ne možemo dobiti hranom, odavno bismo nestali kao vrsta. Istina je skromnija. Kod čoveka se oko 5-15 g glukoze preusmeri u gulonsku kiselinu, smer u metabolizmu koji vodi u sintezu vitamina C, a kod eksperimentalnih životinja tek oko jedan posto ovog puta vodi u stvaranje vitamina C. To znači da bi čoveku trebalo najmanje 50-150 mg vitamina C dnevno [10]. Ispitivanja na životinjama koje ne mogu stvarati vitamin C pokazuju sličan trend.
Linus Pauling i brojni drugi pobornici velikih doza više su razmišljali o vitaminu C kao farmakološkoj intervenciji. Sedamdesetih godina XX veka proširila se popularna ideja zaštite od pro-oksidansa, u kojoj je vitamin C trebao biti univerzalno oružje koje će usporiti proces starenja, smanjiti učestalost infekcija, kao i oboljevanje od kardiovaskularnih bolesti i tumora. Nažalost, on uglavnom nije opravdao takva očekivanja (videti- Klinička upotreba).
Prema National Institutes of Health, preporučeni unos za odraslog muškarca iznosi 90 mg, za žene 75 mg, u trudnoći 85 mg, a tokom dojenja 120 mg. Posebno se i navodi kako je pušačima potrebno 35 mg dnevno više, jer prooksidansi iz dima cigarete smanjuju njegov nivo. Deci od 0 do 6 meseci je potrebno 40 mg, 7-12 meseci 50 mg, 1-3 godine 15 mg, 4-8 godina 25 mg, 9-13 godina 45 mg, 14-18 godina muškarci 75 mg a žene 65 mg. Maksimalni dnevni unos u suplementima ne bi trebao prelaziti 2 g dnevno [44].
Postoje mišljenja kako ove dnevne doze nisu optimalne za celu populaciju. Suplementacija dozom od 100 mg nikada ne izaziva povećanje oksalne kiseline i izlučivanje putem bubrega, a doza od 200 mg se gotovo u potpunosti apsorbuje u sistemu za varenje, a tek u gramskoj dozi dolazi do znatnijeg izlučivanja u bubrezima uz porast oksalne kliseline. Jedna od predloženih alternativa je 200 mg dnevno [30]. Ovakve preporuke temelje se na procenama zdrave populacije. Postoji razmišljanje da se preporuke koriguju zavisno od indeksa telesne težine. Ljudi s povišenim indeksom mogu imati veći rizik od nedostatka čak i uz suplementaciju [45].
Zbog čega nam treba relativno malo vitamina C? Jer ga možemo regenerisati. Enzim glutation uz pomoć dihidroaskorbat reduktaze redukuje oksidovani vitamin C. U tom procesu trošimo glutation, a glutation ćemo redukovati uz pomoć NADH (pročitajte Apsorpcija, distribucija, metabolizam, izlučivanje). Skladištenje u tkivima, kao i reapsorpcija u bubrezima, omogućuju održavanje stabilne koncentracije u krvi u slučaju kratkotrajnog nedostatka u ishrani.
Brojni faktori utiču na nivo vitamina C u telu; ishrana je bitan, ali svakako ne jedini. Detaljnije možete pročitati u citiranoj referenci [46].
- Unos hranom je najbitniji faktor. Smanjen unos voća i povrća treći je po redu uzrok smrti i bolesti na Zemlji [47], ali taj podatak ne smemo olako interpretirati kao da je nedostatak vitamina C treći po redu uzrok (pogledati: Klinička primena). Načini obrade hrane utiču na dostupnost vitamina C, jer ga produženo kuvanje uništava u hrani. Unutar iste grupe namirnica postoje razlike. Skrobom bogate žitarice sadrže daleko manje vitamina C od skrobom bogatog krompira.
- U razvijenim državama unos suplemenata je relativno čest. Ljudi koji koriste vitaminske suplemente imaju neznatan rizik od nedostatka vitamina C, odnosno nižeg nivoa u krvi.
- Socioekonomski status u društvu snažno utiče na nivo vitamina C. Čak jedanaest studija potvrđuje da su siromašniji ljudi više izloženi riziku od nedostatka zbog oskudnijeg odabira namirnica.
- Nivo obrazovanja utiče na nivo vitamina C, jer bolje obrazovani ljudi imaju svest o potrebi zdrave ishrane, i eventualno suplementacije.
- Rasa i nacionalna pripadnost mogu uticati na nivo vitamina C. U jugoistočnoj Aziji Malezijci i Indijci imaju niži nivo od Kineza, verovatno zbog načina ishrane i kuvanja.
- Ljudi koji žive u ustanovama, poput sveštenstva, vojnika, starijih ljudi u domovima, kao i studenata i učenika u domovima imaju veći rizik od nedostatka, zbog jednoličnije ishrane.
- U više zemalja, poput Indije i Francuske, postoji razlika među regijama, ali sam geografski položaj nije jedini faktor. Razlike u dostupnoj hrani, klimi i socioekonomskom statusu mogu biti povezane sa lokacijom.
- Sezonske promene i klima igraju ulogu kroz dostupnost namirnica. U siromašnijim zemljama, snažne zime ili sušna leta povećavaju rizik od nedostatka.
- Zagađenost postaje jedan od centralnih problema planete. Sedam studija potvrdilo je povezanost zagađenja i nedostatka vitamina C. To treba imati na umu, jer su gradovi našeg područja često evropski rekorderi zagađenosti. Smanjenje vitamina C nastaje zbog povećanog oksidativnog stresa, baš kao i kod pušenja.
- Muški pol ima manji nivo od žena, pogotovo u razvijenim zemljama, verovatno zbog veće nemasne mase tela. Studije u starijih ljudi se razlikuju; u nekim studijama nivoi su viši zbog manje nemasne mase, a kod nekih nivoi su manji zbog oskudnije ishrane.
- Pušači, pasivni i aktivni, imaju niže nivoe i treba barem 35 mg više.
- Trudnoća i dojenje povećavaju potrebe za vitaminom C.
- Bolesti poput infekcije povećavaju potrebe za vitaminom C zbog povećanog oksidativnog stresa. Ne postoji konsenzus koliko se povećavaju te potrebe.
Genetski polimorfizmi, odnosno genetske razlike među ljudima, igraju ulogu u dostupnosti vitamina C. SLC23A1 gen kodira SVCT1 protein i postoje genetske razlike u populaciji. Postoje četiri genetska tipa kod kojih se povećava rizik od nedostatka, jer je kod tih ljudi SVCT1 protein manje delotvoran u apsorpciji u crevima i bubrezima. Te su varijante najčešće kod ljudi iz Afrike crne boje kože. Hp2-2 protein veže se za hemoglobin i neke genetske varijante slabije se vežu za njega. To verovatno povećava oksidativni stres i smanjuje nivo vitamina C. Takve mutacije su najčešće u Indiji. Mutacije koje uzrokuju manje efikasni detoksikujući enzim glutation S transferaza, mogu smanjiti nivo vitamina C. Čini se da razlike nisu dramatične. trenutno se vrlo retko unapred testiraju takve genetske varijante i ne postoje smernice za suplementaciju. Genetski polimorfizmi koji utiču na vitamin C rutinski se ne određuju u laboratorijama.

Hrana bogata vitaminom C
Vitamina C najviše ima u svežem voću i povrću, ali skladištenjem njegov nivo opada. Postoje namirnice sa vrlo velikim učešćem vitamina C, poput paprike i brokolija. Neke biljke, poput acerole, toliko su bogate vitaminom C da su njihovi ekstrakti ili sokovi postali proizvod u suplementaciji. Kuvanje na pari manje smanjuje sadržaj vitamina C.
Izvor vitamina C uglavnom je voće i povrće. Citrusi poput pomorandži i limuna imaju kultni status zbog njihove istorijske primene kao leka za skorbut mornara, ali nisu rekorderi. Paprika i jagoda sadrže više vitamina C od pomorandže i limuna. Sadržaj može zavisiti od svežine namirnice, sorti i uslovima skladištenja, pa navedene vrednosti smatrajte okvirnim. Izvor je Food Data Central.
Namirnica | Sadržaj mg/100 g | Namirnica | Sadržaj mg/100 g |
Paprika, crvena | 142 | Sok od paradajza | 49,8 |
Paprika, zelena | 99,5 | Sok od grejpfruta | 39,4 |
Kelj | 93,4 | Spanać | 30,3 |
Brokoli | 91,3 | Paradajz | 27,2 |
Kivi | 74,7 | Sok od pomorandže | 26,9 |
Jagode | 59,6 | Baby spanać | 26,5 |
Pomorandža | 59,1 | Maline | 23 |
Vitamin C dodaje se često u hranu, bilo radi samog njenog obogaćivanja i povećanja nutritivne vrednosti, bilo kao konzervans. Sokovi i razne pahuljice žitarica namirnice su u koje se često dodaje vitamin C.
Neke namirnice sadrže toliko vitamina C da ih koristimo za suplementaciju umesto sintetskog vitamina C. Sadržaj vitamina C u njima prelazi nekoliko stotina miligrama, do čak gramskih količina na 100 g.
Sok pasjeg (vučjeg) trna (Hippophae rhamnoides), a ne ulje, polako je postao vredan izvor prirodnog vitamina C, koji ozbiljniji proizvođači znaju i određivati, a uz to sadrži i koktel drugih nutrijenata, poput karotenoida. Sadržaj po dnevnom obroku može dosegnuti i 500 mg. Razne vrste šipka (Rosa sp.), odnosno ploda šipka, isto sadrže dosta vitamina C, ali se od njega bazično pravi čaj, a sadržaj vitamina C u njemu jako varira, zavisno od mesta rasta, vrsta i vremenu branja. Acerola (Malpighia emarginata) decenijama je izvor prirodnog vitamina C, ali nju nalazimo na tržištu uglavnom kao ekstrakt. Tu dolazimo do problema. U dodacima ishrani nalazimo ekstrakt šipurka ili acerole sa toliko i toliko vitamina C, i to se prihvata zdravo za gotovo. Problem je što se takvim prirodnim ekstraktima često dodaje sintetski vitamin C. To nije opasno, ali nije etično. Takve sirovine normalno nalazimo na svetskom tržištu, sa opaskom na certifikatu: „zbog varijacije prirodnog materijala, do željenog udela vitamina C može biti dodan USP (sintetski) vitamin C“.
Ekstrakt i prah camu camu (Myrciaria dubia) ploda dugo je već prisutan na tržištu. Sadržaj vitamina C u prahu obično prelazi 1 gram na 100 grama, a kod ekstrakta i više. Terminalia ferdinandiana je australska biljka čiji plod sadrži najmanje dvostruko više vitamina C u odnosu na camu camu, i nema sumnje da će je jednog dana marketing iskoristiti.
Skladištenje smanjuje sadržaj vitamina C. Sok ananasa skladištenjem na sobnoj temperaturi gubi 0,6 mg/100 g dnevno, dovodeći do potpunog raspada za manje od mesec dana [48]. Sok od pomorandže gubi manje vitamina C. Nakon šest meseci, sok pomorandže gubi 18 posto na 18°C i 31 posto na 28°C. Potreban je oprez u interpretaciji, jer sadržaj vitamina C zavisi od metode određivanja [49].
Termička obrada smanjuje količinu vitamina C i to je dovelo do ideje kako bilo kakvo zagrevanje potpuno uništava vitamin C. To nije tačno. Vitamin C je nestabilan na povišenoj temperaturi, ali u povrću i voću vitamin C štite i drugi prirodni antioksidativni molekuli. Kao primer možemo uzeti brokoli. Najpreglednije je rezultate prikazati u tablici. Svi procesi kuvanja trajali su pet minuta.
| Način kuvanja | % gubitka referenca [50] | % gubitka referenca [51] |
| Dinstanje | 38 | - |
| Kuvanje u vodi | 33 | 47 |
| Kuvanje na pari | 0 | 0 |
| Mikrotalasno | 16 | 0 |
| Blanširanje | - | 21 |
Gubitak kuvanjem zavisi od namirnice. Krompir kuvanjem u vodi gubi oko 50 posto vitamina C, a kuvanjem na pari 16 posto vitamina C. Kuvanjem i u vodi i na pari blitva gubi sav vitamin C, a blanširanjem gubi 40 posto. Kod većine namirnica kuvanje na pari i mikrotalasno kuvanje manje smanjuju sadržaj vitamina C. Način kuvanja je bitan kod ljudi koji ne jedu sirovo voće zbog raznih razloga, ili uopšte unose manje voća i povrća u ishrani, pa je kuvanje na pari dostupan i jednostavan način boljeg očuvanja vitamina C.

Klinička upotreba
Postoji ogroman broj kliničkih studija koje su pokušale utvrditi u kojim bolestima bi vitamin C bio koristan u prevenciji ili lečenju. Postoji konsenzus da može biti koristan u prevenciji prehlade kod ljudi koji naporno fizički rade i treniraju, a njegova preventivna primena može smanjiti trajanje prehlade. Nažalost, suplementi vitamina C ne smanjuju rizik od nastanka malignih tumora i kardiovaskularnih bolesti, ali namirnice bogate vitaminom C su zdrave navike koje pomažu u prevenciji niza bolesti. Oralni preparati vitamina C ne leče tumore. Vitamin C može biti potencijalno koristan u manje poznatim indikacijama, kao što je prevencija oštećenja bubrega kontrastnim sredstvima. Glavna vrednost vitamina C je nadoknada kod ljudi s potencijalnim manjkom u ishrani.
Unos vitamina C je neophodan i njegova suplementacija je potrebna u slučaju nedovoljnog unosa hranom. Tu se svi slažu. Kada se otkrila fiziološka uloga vitamina C, postavilo se pitanje bi li suplementacija vitamina C mogla smanjiti od rizik nastanka bolesti ili pomoći u lečenju. Oksidativni stres našao se na optuženičkoj klupi kao glavni uzrok starenja i niza hroničnih bolesti, a vitamin C trebao je ponuditi zaštitu. Započele su brojne kliničke studije koje su trebale odgovoriti na ta pitanja. Pogrešne percepcije, nerazumevanja i bombastične reklame posledica su nerazumevanja tipova studija.
U delu studija promatrao se učinak u prevenciji bolesti vitamina C iz hrane. Pomoću upitnika u ishrani posmatra se prosečan unos vitamina C. Tu nastaje problem, jer hrana bogata vitaminom C ne sadrži samo vitamin C, već i niz drugih nutrijenata. Sveže voće i povrće je sve samo ne kapsula vitamina C, ono je bogato drugim molekulima, poput polifenola i karotenoida, pa je izvor vlakana. U takvim studijama može doći do velikih problema analize, jer se ne može proveriti istinitost svakog sudije studije, kao i niz zbunjujućih faktora (engleski: confounder) koji se mogu prevideti u tim analizama.
Tek se u delu studija koristio vitamin C kao intervencijski lek, kao i u klasičnim kliničkim studijama delotvornosti lekova.
Kardiovaskularne bolesti
Velika metaanaliza utvrdila je kako redovan unos hrane bogate vitaminom C smanjuje rizik od koronarne bolesti srca [52]. Tipičan današnji naslov na portalima bio bi: „Vitamin C leči bolesti srca“. Navedena studija nije intervencija, već analiza kako pojedini nutrijenti iz hrane utiču na rizik, ali ne na lečenje, već nastalog koronarnog oboljenja srca. Sama studija isto tako jasno navodi kako suplementacija ne smanjuje rizik od nastanka koronarnog oboljenja srca. Dakle, redovna ishrana hranom bogatijom vitaminom C smanjuje rizik, ali intervencija čistim vitaminom C ne smanjuje rizik.
Suplementacija vitaminom C ne smanjuje rizik od moždanog udara, infarkta miokarda i smrti izazvane srčanim udarima [53]. Metaanaliza 29 manjih i kratkotrajnih studija (osam nedelja) potvrdila je smanjenje krvnog pritiska s prosečnom suplementacijskom dozom od 500 mg, ali je efekat vrlo mali i verovatno klinički nedovoljan. Prosečno je sistolni pritisak bio 3,84 mmHg niži kod pacijenata koji su koristili vitamin C [54].
Postoje studije vrlo ciljane primene vitamina C u kardiologiji. Metaanaliza jedanaest studija ukazuje na to da vitamin C smanjuje rizik od atrijske fibrilacije nakon operacije srca [55]. U većini studija korištena je doza od 2 grama noć pre operacije i 500 mg do 1 gram dva puta dnevno kroz pet dana.
Maligni tumori
Premda neke studije pokazuju smanjenje oboljevanja od nekih tumora, deo njih, pogotovo placebo kontrolisanih, to ne pokazuje. U velikoj studiji s više od 80 000 ispitanica prosečan dnevni unos od 205 mg vitamina C smanjio je rizik oboljevanja od karcinoma dojke kod žena sa porodičnom istorijom karcinoma dojke, i to čak 63 posto, ali u ishrani, a ne suplementaciji [56]. Druge studije unosa hranom i intervencijom jasne su u zaključku da ne smanjuje rizik oboljevanja od karcinoma dojke [57-59].
Unos hranom ili suplementacija vitaminom C ne smanjuju rizik od karcinoma želuca [60, 61]. Povećani unos hranom i suplementima (>600 mg u odnosu na <100 mg) smanjuje rizik oboljevanja od karcinoma debelog creva, ali nemoguće je do kraja odvojiti uticaj zbunjujućih faktora poput unosa folne kiseline [62]. Povećani unos hranom, ali ne i vitamin C u suplementima, smanjuje rizik od Non-Hodgkinovog limfoma [63].
U slavnoj francuskoj SU.VI.MAX studiji smanjenje rizika opaženo je samo kod muškaraca, ali je opet nemoguće odvojiti uticaj drugih mikronutrijenata. Autori studije smatraju da je glavni doprinos povećani unos beta-karotena, a ne vitamina C [64]. Druge dugogodišnje studije nisu utvrdile smanjenje rizika [65, 66].
Vitamin C nije čarobno sredstvo prevencije malignih tumora i nismo to mogli očekivati u vrlo složenim činiocima i procesima nastanka bolesti.
Zasebno je poglavlje pokušaj lečenja malignih tumora vitaminom C. Još sedamdesetih godina studije su pokazale moguć povoljan učinak [67, 68], dok s druge strane ispitivanja Mayo klinike nisu pokazala učinak na preživljavanje pacijenata [69]. Danas smo svesni razloga. Prva studija uključivala je kombinaciju oralne i intravenske terapije, dok je studija Mayo klinike bila samo oralna terapija. Intravenskom primenom možemo postići 30-70 puta veću koncentraciju u krvi u odnosu na oralni vitamin C (pogledati Apsorpcija, distribucija, metabolizam, izlučivanje). Kod intravenskog vitamina C u tim dozama treba potpuno preokrenuti način razmišljanja. U tako visokim dozama vitamin C je pro-oksidans koji u tumorskim tkivima podiže nivo vodonik peroksida. To je jedan od verovatnih mehanizama delovanja protiv tumora. Vitamin C u fiziološkoj oralnoj dozi i intravenski vitamin dijametralno su suprotnog delovanja.
Kako to izgleda u stvarnom životu? Postoji niz radova u kojima su opisani individualni slučajevi pokušaja lečenja malignih tumora vitaminom C. 1995. godine pacijentkinja stara 51 godine primljena je u bolnicu sa karcinomom bubrega. Radiološkim pregledima nisu nađene metastaze. Nakon odstranjivanja celog bubrega pacijentkinja je upućena kući. Na kontroli u martu 1996. godine utvrđene su višestruke metastaze s progresijom vidljivom i u novembru 1996. Pacijentkinja je upoznata sa situacijom i prisebnog je stava odbila hemoterapiju, koja tada i nije davala puno izgleda, te se odlučila na intravensku terapiju vitaminom C, 65 g dva puta nedeljno kroz deset meseci. U junu 1997. godine metastaza više nije bilo i pacijentkinja je živela normalno sve do 2001., kada joj je na plućima dijagnostifikovan karcinom ne-malih ćelija. Pacijentica je bila hronični pušač. I opet su se lekari i pacijentkinja odlučili na terapiju vitaminom C, ali ovoga puta nije bilo uspeha i pacijentkinja je, usprkos kontinuiranoj terapiji, umrla u oktobru 2002. godine. Iz ovog smo naučili puno – kako doze moraju biti velike i intravenske, kako je pitanje efikasnosti pitanje sreće, odnosno toga kako će individualno pojedini tip tumora odgovarati na terapiju. Pacijentica je razvila dva tipa tumora, jedan koji je potpuno i neočekivano odlično odgovarao na terapiju, i drugi, koji nije reagovao na terapiju i od kojeg je preminula [70].
Što određuje hoće li tumor biti osetljiv na visoke doze vitamina C? Visoke doze vitamina C verovatno deluju stvaranjem vodonik peroksida, jedinjenja koji razgrađuje enzim katalaza. In vitro, osetljivost jedanaest ćelijskih veza zavisi od katalaze. Linije koje nemaju katalazu ili imaju nisku aktivnost, osetljivije su na vitamin C [71]. Osetljivost ćelija karcinoma dojke zavisi od prisustva transportera SVCT-2 kojim vitamin C ulazi u ćeliju [72], a može zavisiti i od aktivnosti TET demetilaze, enzima za čiju je aktivnost potreban vitamin C [73].
Olako proglašavanje visokih doza vitamina C „lekom za rak“ je pogrešno. Dosadašnji nivo dokaza uglavnom se svodi na male studije ili opise individualnih slučajeva, ali očito postoje tumori otporni na terapiju visokom dozom vitamina C [74].
Prehlada
Linus Pauling je stvorio ideju primene vitamina C u prevenciji i lečenju prehlade još 1971. godine, premda je ona nastala i pre toga doba [75]. Mnogi danas gledaju na Paulingovu ideju sa puno kritike i negativnih emocija, ali se trebamo vratiti u kontekst toga vremena. U to doba već se znalo da imunološke ćelije akumuliraju vitamin C i bila je logična pretpostavka klinički ispitati vitamin C. Sprovedene su brojne studije do današnjih dana. Vrlo velika metaanaliza 43 studije prevencije prehlade i 10 studija lečenja u ranoj fazi infekcije rešila je gotovo četiri decenije dugu raspravu. Preventivno korišćenje 250 mg do 2 grama vitamina C ne smanjuje rizik oboljevanja od prehlade. Ali, u pet studija kod maratonaca, skijaša, vojnika u subarktičkim krajevima, odnosno populacije koja je više fizički aktivna od prosečne populacije, vitamin C smanjuje rizik oboljevanja od prehlade za gotovo 50 posto [76]. Redovna suplementacija skromno smanjuje dužinu trajanja prehlade (14 posto kod dece, 8 posto kod odraslih), ali korišćenje vitamina C kao intervencije u ranim fazama bolesti ne smanjuje dužinu trajanja prehlade. Autori zaključuju kako „zbog konzistentnog smanjenja trajanja prehlade redovnom suplementacijom, niske cene i visoke sigurnosti, pacijenti mogu na individualnoj bazi ispitati je li vitamin C povoljan za njih“.
Treba razlikovati prehladu od ozbiljnijih infekcija. Vitamin C kao kratkotrajna intervencija nije smanjivao rizik od smrti i komplikacija kod Covida-19 čak ni intravenskim putem [77, 78].
Drugi sistemi
Vitamin C može smanjiti rizik od kontrastom indukovane nefropatije, ali se čini manje delotvornim od N-acetil-cisteina [79, 80]. U šest manjih studija, oralni vitamin C pokazao se delotvornim u lečenju anemije pacijenata na hemodijalizi uz standardnu terapiju [81]. Oralna doza od 500 mg dnevno tokom pedeset dana može smanjiti rizik od nastanka kompleksnog regionalnog bolnog sindroma tip I nakon preloma zgloba [82]. Kod bolesnika u jedinicama intenzivne medicinske nege vitamin C može smanjiti rizik od smrti i ubrzati oporavak [83]. Pacijenti su primali vitamin C intravenskim putem, ali su doze bile vrlo raznolike, od samo 500 mg dnevno do većih doza od 50 mg/kg dnevno. U AREDS i AREDS2 studijama unos vitamina C (i drugih mikronutrijenata, poput karotenoida) nije smanjio rizik od nastanka katarakte [84, 85].

Oblici vitamina C
Postoji niz oblika vitamina C: čista askorbinska kiselina, njegove soli, esteri, kalcijumova so i lipozomski oblik. Ne postoje uverljive razlike u njihovoj delotvornosti i svi se mogu koristiti kao suplement.
Vitamin C može se proizvesti ekstrakcijom biljaka kao što su acerola ili camu camu, ali najveći broj suplemenata sadrži ono što se naziva „sintetski“ vitamin C. Polazna sirovina za proizvodnju vitamina C je šećer glukoza, koja se dobiva iz biljnih izvora. Za sintezu se koristi Reichstein-Grüssnerov proces, nastao još davne 1933. godine. Glukoza se koristi kako bi se sačuvala hiralnost vitamina C, odnosno dobio vitamin C identičan prirodnom. Godišnje se proizvede više od 150 000 tona vitamina C i oko 40 posto odlazi za potrebe prehrambene industrije, a samo polovina u farmaceutski sektor. Kina se nametnula kao lider odustajanjem europskih i japanskih kompanija od proizvodnje. Sinteza se odvija u nekoliko koraka, i u nekim od njih koristi se mikrobna fermentacija:
- Proces hidrogenacije glukoze kojim nastaje sorbitol
- Fermentacija sorbitola u šećer sorbozu bakterijom Gluconobacter oxydans. Fermentacija se koristi kako bi se sačuvala hiralnost, odnosno prirodno identični vitamin C.
- Zaštita druge, treće i četvrte hidroksilne skupine acetonom uz nastanak diaceton-L-sorboze
- Oksidacija kalijum permanganatom i grejanjem u vodi zbog uklanjanja acetonske zaštite, čime nastaje 2-keto-L-gulonska kiselina.
- Pregradnja 2-keto-L-gulonske kiseline u vitamin C
Sve do devedesetih godina Reichstein-Grüssnerov proces bio je najčešći sintetski put proizvodnje sa prinosom većim od 50 posto. Glavni problem bio je korak 4, koji nije dobar za okolinu, pa se tražila biotehnološka zamena za hemijski proces. Nakon više decenija istraživanja pronađena je bakterija Ketogulonicigenium robustum, koja je uspješno oksidovala sorbitol u sorbozu. Biotehnološko rešenje uklonilo je i korak 3, jer više nije trebala zaštita molekula acetonom. Zanimljivo, bakteriji Ketogulonicigenium robustum treba „pomoć“ druge bakterije, Bacillus megaterium [86]. Dakle, današnja proizvodnja vitamina C je gotovo uveliko biotehnološki proces:
- Proces hidrogenacije glukoze kojim nastaje sorbitol
- Fermentacijom sorbitola u šećer sorbozu bakterijom Gluconobacter oxydans. Fermentacija se koristi kako bi se sačuvala hiralnost, odnosno prirodno identični vitamin C.
- Fermentacijom s Ketogulonicigenium robustum/Bacillus megaterium iz sorboze nastaje 2-keto-L-gulonska kiselina
- Pregradnja 2-keto-L-gulonske kiseline u vitamin C
Shema.
Postoji li razlika između prirodnog i sintetskog vitamina C? Ne, to su identični molekuli, ali imajte na umu da nikada ne treba mešati pojmove „hrana bogata vitaminom C“ i „suplement vitamina C“ ma kojeg da je izvora u suplementu (pogledati Klinička primena). Bioraspoloživost sintetskog vitamina C u suplementima ista je kao u onome iz hrane ili tek neznatno bolja za vitamin C iz suplemenata, što verovatno nije biološki relevantno. Na primer, vitamin C iz suplemenata nešto je bolje bioraspoloživ od vitamina C iz soka pomorandže, ako merimo vitamin C u plazmi, ali nije različit ako ga merimo u leukocitima [87-90].
Budući da postoji zasićenje aktivnog transporta povećanjem oralne doze vitamina C, postulirana je ideja kako bi formulacije sa polaganim otpuštanjem mogle doprineti boljoj raspoloživosti. U teoriji, sporije otpuštanje ne bi brzo zasitilo receptore kojima apsorbujemo vitamin C. Praksa nije potvrdila teoriju: u dve studije nije se pokazala razlika u nivou vitamina C u krvi kod ljudi [91, 92]. Doduše, tablete s dužim vremenom raspadanja (15-60 minuta) pokazuju nešto bolju bioraspoloživost od onih sa trenutnim raspadom, ali vitamin C iz tableta sa dužim vremenom raspadanja od 60 minuta znatno se lošije apsorbuje [93]. Marketinška ideja kako vitamin C vrlo brzo uklanjamo urinom samo je delimično tačna. Količine koje su nam dostatne duže zadržavamo u tkivima (pogledati Apsorpcija, distribucija, metabolizam, izlučivanje), dok višak brzo uklanjamo. Praktična korist oblika vitamina C sa vremenskim otpuštanjem verovatno nije potkrepljena evolucijom, jer ljudi imaju obroke, a ne kontinuirano hranjenje.
Soli askorbinske kiseline, među kojima su natrijum i kalijum askorbat, vrlo su popularne u internet svetu već nekoliko godina. Njihova prednost je blaga alkalnost, pa teoretski mogu biti bolje kod pacijenata koji imaju želučane tegobe poput GERB-a. Mešanje sode bikarbone i vitamina C kućni je način pravljenja natrijum askorbata. Natrijum askorbat nije „lek za rak“, bez obzira na broj objava na društvenim mrežama zadnjih nekoliko godina. Natrijumove i kalijumove soli askorbinske kiseline verovatno nisu bolje bioraspoložive, jer trenutno nedostaju studije koje bi to potvrdile. Kalcijumova so askorbinske kiseline sa trenonatom i dehidroaskorbinskom kiselinom ima svoj komercijalni naziv „Ester-C“. Ne treba mešati ovaj naziv sa esterima masne kiseline i vitamina C; Ester-C hemijski može zbuniti svojim nazivom estera koji to nije. Zna se reklamirati kao superiorno bioraspoloživ. Jedna studija to ne potvrđuje [94], a u drugoj studiji je primećen diskretno veći AUC: 7.73 ± 3.12 µg/mL za Ester-C versus 6.37 ± 2.26 µg/mL za askorbinsku kiselinu unutar 24 sata, ali nije bio značajan za ukupni AUC, koji uključuje vremena i nakon 24 sata. U leukocitima razlika je bila vrlo diskretna i nije bila statistički značajna. Čini se da su autori pokušali stvoriti kreativne grafičke prikaze kako bi se dobio vizualni dojam razlike, a ne objasniti biološke implikacije tih razlika [95]. Ostaje za utehu da se kalcijumova so možda nešto bolje podnosi od askorbinske kiseline, ali samo jedna studija na dve skupine po 25 ispitanika potvrđuje tu tvrdnju [96]. Birate li neki oblik soli vitamina C, a pazite na unos natrijuma, i radije koristite kalijumovu ili kalcijumovu so.
Pravi esteri vitamina C i masnih kiselina poput askorbil-palmitata razvijeni su pre nekoliko decenija kao lipofilniji oblik vitamina C, da bi se lakše koristio u prehrambenoj i kozmetičkoj industriji. In vitro podaci govorili su u prilog mogućoj boljoj bioraspoloživosti, koja nije potvrđena kod ljudi [97]. Flavonoidi se nalaze u sastavu voća i povrća zajedno s vitaminom C i organskim kiselinama. Postojala su velika očekivanja od bioflavonoida zbog njihove in vitro interakcije i sinergije antioksidativnog delovanja sa vitaminom C. Gledajući rezultate šest studija bioraspoloživosti, čini se da bioflavonoidi ne povećavaju bioraspoloživost vitamina C [87].
Postojala su velika očekivanja od lipozomalnog vitamina C. Primena lipozoma i emulgovanih sastava za poboljšanje bioraspoloživosti nije novost u farmaceutskoj tehnologiji, i postoji niz lekova i prirodnih supstanci u kojima je taj koncept uspešno primenjen, uključujući ciklosporin i kvercetin [98, 99]. Jedan od potencijalnih ciljeva formulacija lipozomalnog vitamina C je dostizanje nivoa u krvi uporedivih sa intravenskom primenom. Taj cilj nije postignut i lipozomalni vitamin C daleko zaostaje za istom intravenskom dozom [39]. Dizajn citirane studije kao da je odražavao preterani optimizam istraživača koji su koristili dozu od 4 grama vitamina C, uskrativši nas za informaciju u kojoj meri niže doze lipozomalnog vitamina C mogu biti bolje u odnosu na običnu askorbinsku kiselinu. Lipozomalni vitamin C u toj je studiji pokazao AUC 10.3 ± 0.9 mg/dL h, dok je AUC obične askorbinske kiseline bio 7.6 ± 0.4 mg/dL h. Ako realno gledamo, tridesetak posto veća bioraspoloživost čini se neprimerenom znatno većem postotku cene finalnih proizvoda. Poljski stručnjaci su napravili korektnu studiju i prikazali kvalitetnije podatke s aspekta farmaceutske tehnologije, ali su koristili čak deset grama lipozomske formulacije u poređenju sa istom dozom obične askorbinske kiseline. Lipozomalni oblik bio je bolje bioraspoloživ: najviša koncentracija lipozomalnog bila je 303 µmol/l, a običnog vitamina C 180 µmol/l; AUC liposomalnog 81 570 µmol/l min, a običnog 45 330 µmol/l min [100]. Nešto realističnija doza od 1 grama lipozomalnog vitamina C bila je 1,77 puta bolje bioraspoloživa od obične askorbinske kiseline [101]. Znatno bolji rezultat postignut je kombinacijom lipozomalnog vitamina C u hidrogelu glukomanana piskavice (Trigonella foenum-graecum), koji je bio sedam puta bolje bioraspoloživ [102]. S lipozomalnim vitaminom C postavlja se jedno pitanje: koja je realna klinička prednost postizanja nešto većih koncentracija u krvi, a koje su ionako manje od onih postignutih intravenskom primenom? Vitamin C opšte rečeno nema većih problema sa bioraspoloživošću doza potrebnih za fiziološku funkciju u organizmu. Koliko takav pristup opravdava znatno veću cenu konačnog proizvoda? Za lipozomalni vitamin C nedostaje nam kvalitetna studija u celom rasponu doza od 100 mg naviše, ali i dokaz realne kliničke prednosti nešto većih doza u krvi.
Interakcije sa lekovima
Postoji vrlo nizak rizik od interakcija lekova i vitamina C. Relativno mala doza vitamina C (100 mg) pomaže boljem uklanjanju gvožđa tokom lečenja deferoksaminom kod pacijenata s β-talasemijom [103]. Oralna doza od 2 grama vitamina C može povećati apsorpciju aluminijuma iz antacida koji ga sadrže. Oprez je potreba u slučaju smanjene funkcije bubrega i istovremene primene aluminijskih antacida i većih doza vitamina C [104]. Male studije upućivale su na moguće povišenje nivoa etinil-estradiola kod istovremene suplementacije vitaminom C, no ta interakcija nije potvrđena u većoj studiji [105]. Postoji jedna starija studija u kojoj je 900 mg acetil-salicilne kiseline smanjivalo apsorpciju vitamina C, ali ona kasnije nije potvrđena, niti je primećen nedostatak vitamina C kod hronične primene manjih doza acetil-salicilne kiseline [106]. Vitamin C mogu smanjiti porast HDL holesterola izazvan danas zastarelom kombinacijom simvas* *tatina i niacina, što za sada nije primećeno sa samim statinima bez niacina [107]. Godine 2008. objavljen je rad in vitro i in vivo studije potencijalnog antagonističkog delovanja vitamina C na lekove koji se koriste u lečenju malignih tumora [108]. On je raširio strah do koje mere vitamin C može smanjiti delovanje lekova protiv tumora. Taj je rad imao nekoliko metodoloških pogrešaka, uključujući i korišćenje dehidroaskorbinske kiseline umesto redukovane askorbinske kiseline. Obzirom na to da je nivo vitamina C dobro kontrolisan, oralni preparati sa suplementacijskim dozama verovatno ne predstavljaju problem [109]. Nadalje, vitamin C je nužan za našu fiziologiju, što uključuje i onkološke pacijente na terapiji. Interakcija sa varfarinom je malo verovatna i opisana je tek u nekoliko slučajeva, ali nije sigurno u kojoj meri je zaista vitamin C bio uzrok promene PV-INR [110, 111].
- Bown, S., SCURVY: How a surgeon, a mariner, and a gentleman solved the greatest medical mystery of the age of sail. 2021, [S.l.]: HISTORY PRESS.
- Bierman, A. and J. Burnby, The incidence of scurvy at sea and its treatment. Revue d'Histoire de la Pharmacie, 1996: p. 339-346.
- The Observations of Sir Richard Hawkins, Knight, in his Voyage into the South Sea, Anno Domini 1593. Nutrition Reviews, 1986. 44(11): p. 370-371.
- Martini, E., How did Vasco da Gama sail for 16 weeks without developing scurvy? The Lancet, 2003. 361(9367): p. 1480.
- Woodall, J., The surgions mate. 1617, London: Printed by Edward Griffin for Laurence Lisle, at the Tygers-head in Pauls Church-yard.
- Carpenter, K.J., The discovery of vitamin C. Ann Nutr Metab, 2012. 61(3): p. 259-64.
- MacGillivray, N., The Scottish Scurvy Epidemic of 1847. J R Coll Physicians Edinb, 2020. 50(4): p. 444-450.
- Grzybowski, A. and K. Pietrzak, Albert Szent-Györgyi (1893-1986): The scientist who discovered vitamin C. Clinics in Dermatology, 2013. 31(3): p. 327-331.
- Kumar, D., R. E. Mains, and B. A. Eipper, 60 YEARS OF POMC: From POMC and α-MSH to PAM, molecular oxygen, copper, and vitamin C. J Mol Endocrinol, 2016. 56(4): p. T63-76.
- Handbook of vitamins. 2007, Boca Raton: CRC Press : Taylor & Francis.
- Strowitzki, M. J., E. P. Cummins, and C. T. Taylor, Protein Hydroxylation by Hypoxia-Inducible Factor (HIF) Hydroxylases: Unique or Ubiquitous? Cells, 2019. 8(5).
- Liu, X., et al., Ascorbic Acid in Epigenetic Reprogramming. Curr Stem Cell Res Ther, 2022. 17(1): p. 13-25.
- Padayatty, S. J. and M. Levine, Vitamin C: the known and the unknown and Goldilocks. Oral Dis, 2016. 22(6): p. 463-93.
- Van 't Erve, T. J., Strategies to decrease oxidative stress biomarker levels in human medical conditions: A meta-analysis on 8-iso-prostaglandin F2α. Redox Biology, 2018. 17: p. 284-296.
- Bunpo, P. and T. G. Anthony, Ascorbic acid supplementation does not alter oxidative stress markers in healthy volunteers engaged in a supervised exercise program. Appl Physiol Nutr Metab, 2016. 41(2): p. 175-80.
- Retana-Ugalde, R., et al., High dosage of ascorbic acid and alpha-tocopherol is not useful for diminishing oxidative stress and DNA damage in healthy elderly adults. Ann Nutr Metab, 2008. 52(2): p. 167-73.
- Cangemi, R., et al., Oxidative stress-mediated arterial dysfunction in patients with metabolic syndrome: Effect of ascorbic acid. Free Radic Biol Med, 2007. 43(5): p. 853-9.
- Ristow, M., et al., Antioxidants prevent health-promoting effects of physical exercise in humans. Proc Natl Acad Sci U S A, 2009. 106(21): p. 8665-70.
- Stanger, O., et al., Antioxidant supplementation attenuates oxidative stress in patients undergoing coronary artery bypass graft surgery. Tohoku J Exp Med, 2014. 232(2): p. 145-54.
- Righi, N. C., et al., Effects of vitamin C on oxidative stress, inflammation, muscle soreness, and strength following acute exercise: meta-analyses of randomized clinical trials. Eur J Nutr, 2020. 59(7): p. 2827-2839.
- Abdollahzad, H., et al., Effect of vitamin C supplementation on oxidative stress and lipid profiles in hemodialysis patients. Int J Vitam Nutr Res, 2009. 79(5-6): p. 281-7.
- Hamilton, I. M., et al., Interactions between vitamins C and E in human subjects. Br J Nutr, 2000. 84(3): p. 261-7.
- Duarte, T. L. and J. Lunec, Review: When is an antioxidant not an antioxidant? A review of novel actions and reactions of vitamin C. Free Radic Res, 2005. 39(7): p. 671-86.
- Lykkesfeldt, A. C. C. J., Vitamin C in Health and Disease. 2018.
- Akram, N. A., F. Shafiq, and M. Ashraf, Ascorbic Acid-A Potential Oxidant Scavenger and Its Role in Plant Development and Abiotic Stress Tolerance. Frontiers in Plant Science, 2017. 8.
- Drouin, G., J. R. Godin, and B. Pagé, The genetics of vitamin C loss in vertebrates. Curr Genomics, 2011. 12(5): p. 371-8.
- Yang, H., Conserved or lost: molecular evolution of the key gene GULO in vertebrate vitamin C biosynthesis. Biochem Genet, 2013. 51(5-6): p. 413-25.
- Maxfield, L., Crane, JS., Vitamin C Deficiency, in StatPearls [Internet]. 2022, StatPearls Publishing: Treasure Island (FL).
- Lykkesfeldt, J. and P. Tveden-Nyborg, The Pharmacokinetics of Vitamin C. Nutrients, 2019. 11(10).
- Levine, M., et al., Vitamin C pharmacokinetics in healthy volunteers: evidence for a recommended dietary allowance. Proc Natl Acad Sci U S A, 1996. 93(8): p. 3704-9.
- Smirnoff, N., Ascorbic acid metabolism and functions: A comparison of plants and mammals. Free Radic Biol Med, 2018. 122: p. 116-129.
- Gerster, H., No contribution of ascorbic acid to renal calcium oxalate stones. Ann Nutr Metab, 1997. 41(5): p. 269-82.
- Crivelli, J. J., et al., Contribution of Dietary Oxalate and Oxalate Precursors to Urinary Oxalate Excretion. Nutrients, 2020. 13(1).
- Curhan, G. C., et al., A prospective study of the intake of vitamins C and B6, and the risk of kidney stones in men. J Urol, 1996. 155(6): p. 1847-51.
- Curhan, G. C., et al., Intake of vitamins B6 and C and the risk of kidney stones in women. J Am Soc Nephrol, 1999. 10(4): p. 840-5.
- Taylor, E. N., M. J. Stampfer, and G. C. Curhan, Dietary factors and the risk of incident kidney stones in men: new insights after 14 years of follow-up. J Am Soc Nephrol, 2004. 15(12): p. 3225-32.
- Jiang, K., et al., Ascorbic Acid Supplements and Kidney Stones Incidence Among Men and Women: A systematic review and meta-analysis. Urol J, 2019. 16(2): p. 115-120.
- Jacob, R. A. and G. Sotoudeh, Vitamin C function and status in chronic disease. Nutr Clin Care, 2002. 5(2): p. 66-74.
- Davis, J. L., et al., Liposomal-encapsulated Ascorbic Acid: Influence on Vitamin C Bioavailability and Capacity to Protect Against Ischemia-Reperfusion Injury. Nutr Metab Insights, 2016. 9: p. 25-30.
- Duconge, J., et al., Pharmacokinetics of vitamin C: insights into the oral and intravenous administration of ascorbate. P R Health Sci J, 2008. 27(1): p. 7-19.
- Schoenfeld, J. D., et al., Pharmacological Ascorbate as a Means of Sensitizing Cancer Cells to Radio-Chemotherapy While Protecting Normal Tissue. Semin Radiat Oncol, 2019. 29(1): p. 25-32.
- Nielsen, T. K., et al., Elimination of ascorbic acid after high-dose infusion in prostate cancer patients: a pharmacokinetic evaluation. Basic Clin Pharmacol Toxicol, 2015. 116(4): p. 343-8.
- Stephenson, C. M., et al., Phase I clinical trial to evaluate the safety, tolerability, and pharmacokinetics of high-dose intravenous ascorbic acid in patients with advanced cancer. Cancer Chemother Pharmacol, 2013. 72(1): p. 139-46.
- Food and P.o.D.A.I.o.M.S. Nutrition Board Staff, Dietary Reference Intakes for Vitamin C, Vitamin E, Selenium and Carotenoids : A Report of the Panel on Dietary Antioxidants and Related Compounds, Subcommittees on Upper Reference Levels of Nutrients and of Interpretation and Use of Dietary Reference Intakes and the Standing Committee on the Scientific Evaluation of Dietary Reference Intakes, Food and Nutrition Board, Institute of Medicine. 2000.
- Block, G., et al., Body weight and prior depletion affect plasma ascorbate levels attained on identical vitamin C intake: a controlled-diet study. J Am Coll Nutr, 1999. 18(6): p. 628-37.
- Carr, A. C. and S. Rowe, Factors Affecting Vitamin C Status and Prevalence of Deficiency: A Global Health Perspective. Nutrients, 2020. 12(7).
- Health effects of dietary risks in 195 countries, 1990-2017: a systematic analysis for the Global Burden of Disease Study 2017. Lancet, 2019. 393(10184): p. 1958-1972.
- Uckiah, A., D. Goburdhun, and A. Ruggoo, Vitamin C content during processing and storage of pineapple. Nutrition & Food Science, 2009. 39(4): p. 398-412.
- Galani, J. H. Y., et al., Storage of Fruits and Vegetables in Refrigerator Increases their Phenolic Acids but Decreases the Total Phenolics, Anthocyanins and Vitamin C with Subsequent Loss of their Antioxidant Capacity. Antioxidants (Basel), 2017. 6(3).
- Yuan, G. F., et al., Effects of different cooking methods on health-promoting compounds of broccoli. J Zhejiang Univ Sci B, 2009. 10(8): p. 580-8.
- Lee, S., et al., Effect of different cooking methods on the content of vitamins and true retention in selected vegetables. Food Sci Biotechnol, 2018. 27(2): p. 333-342.
- Ye, Z. and H. Song, Antioxidant vitamins intake and the risk of coronary heart disease: meta-analysis of cohort studies. Eur J Cardiovasc Prev Rehabil, 2008. 15(1): p. 26-34.
- Ye, Y., J. Li, and Z. Yuan, Effect of antioxidant vitamin supplementation on cardiovascular outcomes: a meta-analysis of randomized controlled trials. PLoS One, 2013. 8(2): p. e56803.
- Juraschek, S. P., et al., Effects of vitamin C supplementation on blood pressure: a meta-analysis of randomized controlled trials. Am J Clin Nutr, 2012. 95(5): p. 1079-88.
- Baker, W. L. and C. I. Coleman, Meta-analysis of ascorbic acid for prevention of postoperative atrial fibrillation after cardiac surgery. Am J Health Syst Pharm, 2016. 73(24): p. 2056-2066.
- Zhang, S., et al., Dietary carotenoids and vitamins A, C, and E and risk of breast cancer. J Natl Cancer Inst, 1999. 91(6): p. 547-56.
- Hutchinson, J., et al., Vitamin C intake from diary recordings and risk of breast cancer in the UK Dietary Cohort Consortium. Eur J Clin Nutr, 2012. 66(5): p. 561-8.
- Nagel, G., et al., Dietary beta-carotene, vitamin C and E intake and breast cancer risk in the European Prospective Investigation into Cancer and Nutrition (EPIC). Breast Cancer Res Treat, 2010. 119(3): p. 753-65.
- Roswall, N., et al., Micronutrient intake and breast cancer characteristics among postmenopausal women. Eur J Cancer Prev, 2010. 19(5): p. 360-5.
- Jenab, M., et al., Plasma and dietary vitamin C levels and risk of gastric cancer in the European Prospective Investigation into Cancer and Nutrition (EPIC-EURGAST). Carcinogenesis, 2006. 27(11): p. 2250-7.
- Taylor, P.R., et al., Prevention of esophageal cancer: the nutrition intervention trials in Linxian, China. Linxian Nutrition Intervention Trials Study Group. Cancer Res, 1994. 54(7 Suppl): p. 2029s-2031s.
- Park, Y., et al., Intakes of vitamins A, C, and E and use of multiple vitamin supplements and risk of colon cancer: a pooled analysis of prospective cohort studies. Cancer Causes Control, 2010. 21(11): p. 1745-57.
- Thompson, C. A. and J. R. Cerhan, Fruit and vegetable intake and survival from non-Hodgkin lymphoma: does an apple a day keep the doctor away? Leuk Lymphoma, 2010. 51(6): p. 963-4.
- Hercberg, S., et al., The SU.VI.MAX Study: a randomized, placebo-controlled trial of the health effects of antioxidant vitamins and minerals. Arch Intern Med, 2004. 164(21): p. 2335-42.
- Gaziano, J. M., et al., Vitamins E and C in the prevention of prostate and total cancer in men: the Physicians' Health Study II randomized controlled trial. Jama, 2009. 301(1): p. 52-62.
- Lin, J., et al., Vitamins C and E and beta carotene supplementation and cancer risk: a randomized controlled trial. J Natl Cancer Inst, 2009. 101(1): p. 14-23.
- Cameron, E. and A. Campbell, The orthomolecular treatment of cancer. II. Clinical trial of high-dose ascorbic acid supplements in advanced human cancer. Chem Biol Interact, 1974. 9(4): p. 285-315.
- Cameron, E. and L. Pauling, Supplemental ascorbate in the supportive treatment of cancer: Prolongation of survival times in terminal human cancer. Proc Natl Acad Sci U S A, 1976. 73(10): p. 3685-9.
- Moertel, C. G., et al., High-dose vitamin C versus placebo in the treatment of patients with advanced cancer who have had no prior chemotherapy. A randomized double-blind comparison. N Engl J Med, 1985. 312(3): p. 137-41.
- Padayatty, S. J., et al., Intravenously administered vitamin C as cancer therapy: three cases. Cmaj, 2006. 174(7): p. 937-42.
- Klingelhoeffer, C., et al., Natural resistance to ascorbic acid induced oxidative stress is mainly mediated by catalase activity in human cancer cells and catalase-silencing sensitizes to oxidative stress. BMC Complement Altern Med, 2012. 12: p. 61.
- Hong, S. W., et al., SVCT-2 in breast cancer acts as an indicator for L-ascorbate treatment. Oncogene, 2013. 32(12): p. 1508-17.
- Vissers, M. C. M. and A.B. Das, Potential Mechanisms of Action for Vitamin C in Cancer: Reviewing the Evidence. Front Physiol, 2018. 9: p. 809.
- Jacobs, C., et al., Is there a role for oral or intravenous ascorbate (vitamin C) in treating patients with cancer? A systematic review. Oncologist, 2015. 20(2): p. 210-23.
- Pauling, L., The significance of the evidence about ascorbic acid and the common cold. Proc Natl Acad Sci U S A, 1971. 68(11): p. 2678-81.
- Hemilä, H. and E. Chalker, Vitamin C for preventing and treating the common cold. Cochrane Database Syst Rev, 2013. 2013(1): p. Cd000980.
- Ao, G., et al., Intravenous vitamin C use and risk of severity and mortality in COVID-19: A systematic review and meta-analysis. Nutr Clin Pract, 2022. 37(2): p. 274-281.
- Rawat, D., et al., Vitamin C and COVID-19 treatment: A systematic review and meta-analysis of randomized controlled trials. Diabetes Metab Syndr, 2021. 15(6): p. 102324.
- Feng, Y., et al., N-acetylcysteine versus ascorbic acid or N-acetylcysteine plus ascorbic acid in preventing contrast-induced nephropathy: A meta-analysis. Nephrology (Carlton), 2018. 23(6): p. 530-538.
- Xu, Y., et al., Vitamins for Prevention of Contrast-induced Acute Kidney Injury: A Systematic Review and Trial Sequential Analysis. Am J Cardiovasc Drugs, 2018. 18(5): p. 373-386.
- Deved, V., et al., Ascorbic acid for anemia management in hemodialysis patients: a systematic review and meta-analysis. Am J Kidney Dis, 2009. 54(6): p. 1089-97.
- Aïm, F., et al., Efficacy of vitamin C in preventing complex regional pain syndrome after wrist fracture: A systematic review and meta-analysis. Orthop Traumatol Surg Res, 2017. 103(3): p. 465-470.
- Shrestha, D. B., et al., Vitamin C in Critically Ill Patients: An Updated Systematic Review and Meta-Analysis. Nutrients, 2021. 13(10).
- A randomized, placebo-controlled, clinical trial of high-dose supplementation with vitamins C and E and beta carotene for age-related cataract and vision loss: AREDS report no. 9. Arch Ophthalmol, 2001. 119(10): p. 1439-52.
- Chew, E. Y., et al., Lutein/zeaxanthin for the treatment of age-related cataract: AREDS2 randomized trial report no. 4. JAMA Ophthalmol, 2013. 131(7): p. 843-50.
- Pappenberger, G. and H. P. Hohmann, Industrial production of L-ascorbic Acid (vitamin C) and D-isoascorbic acid. Adv Biochem Eng Biotechnol, 2014. 143: p. 143-88.
- Carr, A. C. and M. C. Vissers, Synthetic or food-derived vitamin C--are they equally bioavailable? Nutrients, 2013. 5(11): p. 4284-304.
- Gregory, J. F., 3rd, Ascorbic acid bioavailability in foods and supplements. Nutr Rev, 1993. 51(10): p. 301-3.
- Mangels, A. R., et al., The bioavailability to humans of ascorbic acid from oranges, orange juice and cooked broccoli is similar to that of synthetic ascorbic acid. J Nutr, 1993. 123(6): p. 1054-61.
- Pelletier, O. and M. O. Keith, Bioavailability of synthetic and natural ascorbic acid. J Am Diet Assoc, 1974. 64(3): p. 271-5.
- Nyyssönen, K., et al., Effect of supplementation of smoking men with plain or slow release ascorbic acid on lipoprotein oxidation. Eur J Clin Nutr, 1997. 51(3): p. 154-63.
- Viscovich, M., J. Lykkesfeldt, and H. E. Poulsen, Vitamin C pharmacokinetics of plain and slow release formulations in smokers. Clin Nutr, 2004. 23(5): p. 1043-50.
- Bhagavan, H. N. and B. I. Wolkoff, Correlation between the disintegration time and the bioavailability of vitamin C tablets. Pharm Res, 1993. 10(2): p. 239-42.
- Johnston, C. S. and B. Luo, Comparison of the absorption and excretion of three commercially available sources of vitamin C. J Am Diet Assoc, 1994. 94(7): p. 779-81.
- Mitmesser, S. H., et al., Determination of plasma and leukocyte vitamin C concentrations in a randomized, double-blind, placebo-controlled trial with Ester-C(®). Springerplus, 2016. 5(1): p. 1161.
- Gruenwald, J., et al., Safety and tolerance of ester-C compared with regular ascorbic acid. Adv Ther, 2006. 23(1): p. 171-8.
- De Ritter, E., N. Cohen, and S. H. Rubin, Physiological availability of dehydro-L-ascorbic acid and palmitoyl-L-ascorbic acid. Science, 1951. 113(2944): p. 628-31.
- Yang, S. G., et al., Stable bioavailability of cyclosporin A, regardless of food intake, from soft gelatin capsules containing a new self-nanoemulsifying formulation. Int J Clin Pharmacol Ther, 2006. 44(5): p. 233-9.
- Riva, A., et al., Improved Oral Absorption of Quercetin from Quercetin Phytosome®, a New Delivery System Based on Food Grade Lecithin. Eur J Drug Metab Pharmacokinet, 2019. 44(2): p. 169-177.
- Łukawski, M., et al., New oral liposomal vitamin C formulation: properties and bioavailability. J Liposome Res, 2020. 30(3): p. 227-234.
- Gopi, S. and P. Balakrishnan, Evaluation and clinical comparison studies on liposomal and non-liposomal ascorbic acid (vitamin C) and their enhanced bioavailability. J Liposome Res, 2021. 31(4): p. 356-364.
- Joseph, A., et al., Surface-engineered liposomal particles of calcium ascorbate with fenugreek galactomannan enhanced the oral bioavailability of ascorbic acid: a randomized, double-blinded, 3-sequence, crossover study. RSC Adv, 2021. 11(60): p. 38161-38171.
- Elalfy, M. S., et al., Role of vitamin C as an adjuvant therapy to different iron chelators in young β-thalassemia major patients: efficacy and safety in relation to tissue iron overload. Eur J Haematol, 2016. 96(3): p. 318-26.
- Domingo, J. L., et al., Effect of ascorbic acid on gastrointestinal aluminium absorption. Lancet, 1991. 338(8780): p. 1467.
- Zamah, N. M., et al., Absence of an effect of high vitamin C dosage on the systemic availability of ethinyl estradiol in women using a combination oral contraceptive. Contraception, 1993. 48(4): p. 377-91.
- Basu, T. K., Vitamin C-aspirin interactions. Int J Vitam Nutr Res Suppl, 1982. 23: p. 83-90.
- Brown, B. G., et al., Simvastatin and niacin, antioxidant vitamins, or the combination for the prevention of coronary disease. N Engl J Med, 2001. 345(22): p. 1583-92.
- Heaney, M. L., et al., Vitamin C antagonizes the cytotoxic effects of antineoplastic drugs. Cancer Res, 2008. 68(19): p. 8031-8.
- Levine, M., M.G. Espey, and Q. Chen, Losing and finding a way at C: new promise for pharmacologic ascorbate in cancer treatment. Free Radic Biol Med, 2009. 47(1): p. 27-9.
- Feetam, C. L., R. H. Leach, and M. J. Meynell, Lack of a clinically important interaction between warfarin and ascorbic acid. Toxicology and Applied Pharmacology, 1975. 31(3): p. 544-547.
- Sattar, A., J. E. Willman, and R. Kolluri, Possible warfarin resistance due to interaction with ascorbic acid: case report and literature review. Am J Health Syst Pharm, 2013. 70(9): p. 782-6.

Autor: Dr. sc. Stribor Marković,
magistar farmacije
Najteži dio posla bio je pomiriti dva svijeta, stručni i laički. Htio sam napraviti informativni sadržaj za medicinsku struku, od liječnika i farmaceuta do nutricionista, u kojem bi mogli zaroniti do one dubine do koje sami žele.